近日,公司李中伟教授团队在中科院医学一区期刊《Genes & Diseases》(小类:生化与分子生物学一区;即时IF:14.2)发表题为《Protein arginine methylation and ubiquitination: A prominent crosstalk and its functions in cancer》的综述论文。

文章封面
该综述系统回顾了近年来蛋白质精氨酸甲基化与泛素化的互作研究,着重阐述了二者交叉作用在肿瘤多种关键生物学过程中的核心机制,并探讨了该交叉作用在癌症治疗领域未来研究方向,为相关基础研究及抗癌药物研发提供了新视角。
癌症治疗在医学领域仍面临重大挑战,这主要源于癌细胞与正常细胞在关键调控机制上高度相似性与显著病理差异。PRMTs家族成员对癌症恶性进展具有显著影响,精氨酸甲基化可影响蛋白质功能及相互作用,从而参与癌症的表观遗传调控。泛素化系统通过特异性标记作用调节靶蛋白的稳定性与活性。值得注意的是,这两种翻译后修饰系统不仅在癌症发展中起关键作用,还构成复杂的相互作用网络:甲基化可通过影响泛素酶复合体活性改变癌基因的降解效率,而泛素化过程则能反向调控蛋白质精氨酸甲基转移酶(PRMTs)的稳定性。这种动态相互作用在癌症微环境重塑及治疗耐药性发展等关键病理过程中具有决定性意义。不同的甲基化模式会影响泛素连接酶的识别与募集效率,从而双向调控关键调控因子的稳定性及功能活性。在表观遗传层面,特定甲基化修饰可改变染色质复合物的空间构象,进而影响DNA损伤应答系统的效率。类似地,甲基转移酶与去泛素化酶协同修饰机制可作为致癌信号通路持续激活的分子基础。这种多维度修饰相互作用网络为理解癌症发生机制提供了新视角。
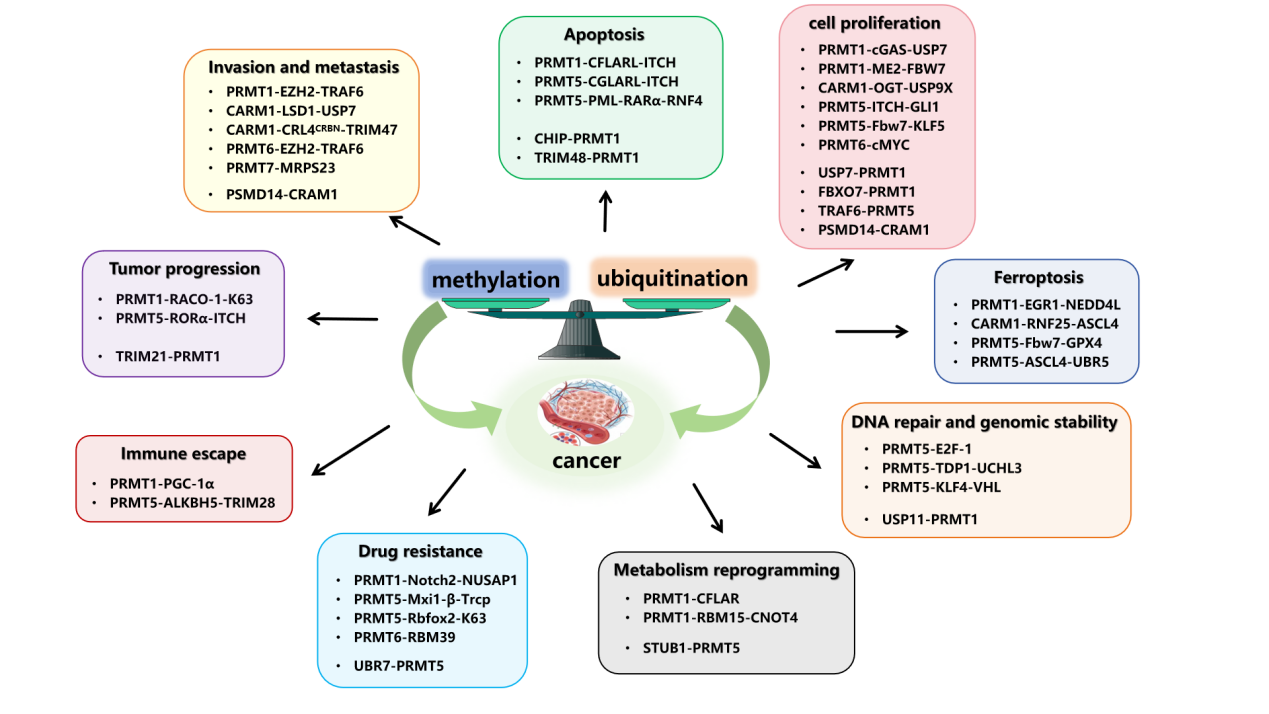
原文配图
基础医学2023级病理生理学硕士研究生张澳与青年教师朱久玲为论文共同第一作者,tyc8722太阳集团李曙教授与李中伟教授为论文共同通讯作者,tyc8722太阳集团为该论文第一完成单位及第一通讯单位。该研究得到了国家自然科学基金面上项目、安徽省高校自然科学研究杰出青年项目、tyc8722太阳集团高层次人才启动基金等项目的支持。(朱久玲/文,周嘉雯供图)
 联系地址:中国安徽省芜湖市弋江区文昌西路22号
联系地址:中国安徽省芜湖市弋江区文昌西路22号 联系方式:0553-3932459 邮编:241002
联系方式:0553-3932459 邮编:241002 举报电话:0553-3932753 邮箱:jcjw@wnmc.com.cn
举报电话:0553-3932753 邮箱:jcjw@wnmc.com.cn